Deshabilitar las enzimas clave supera las limitaciones previas para bloquear la angiogénesis y puede fundamentar las estrategias de tratamiento del cáncer
QUÉ:
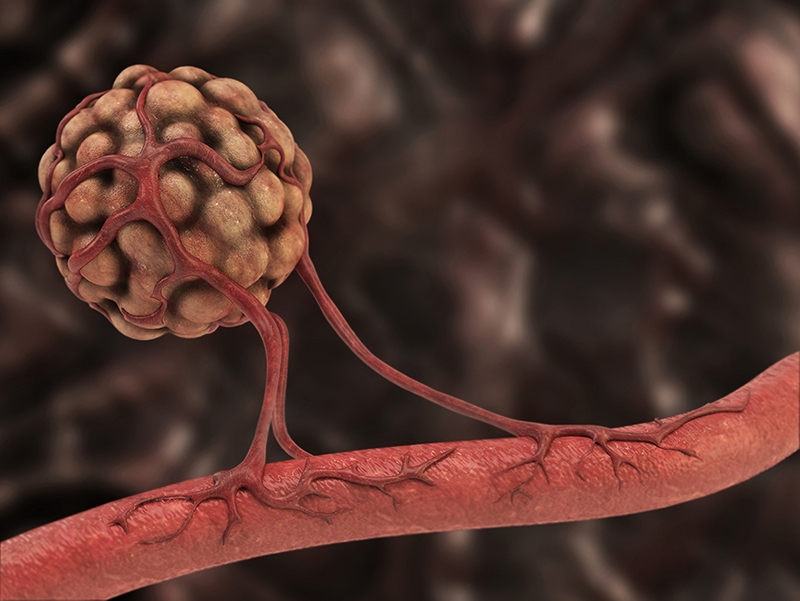
Los científicos de los Institutos Nacionales de la Salud y otras instituciones han ideado una nueva estrategia para evitar que los tumores desarrollen los nuevos vasos sanguíneos que necesitan para crecer. El bloqueo de las moléculas que estimulan el crecimiento de nuevos vasos sanguíneos (angiogénesis), que alguna vez se pensó que era extremadamente prometedor para el tratamiento del cáncer, ha resultado ineficaz porque las células tumorales responden produciendo más moléculas estimuladoras. La nueva estrategia consiste en deshabilitar las enzimas clave que reponen la molécula que las células necesitan para las reacciones que sostienen el crecimiento de nuevos vasos. El equipo de investigación fue dirigido por Brant M. Weinstein, Ph.D., jefe de la División de Organogénesis de Vertebrados del Instituto Nacional de Salud Infantil y Desarrollo Humano (NICHD) Eunice Kennedy Shriver de los NIH. El estudio aparece en Nature Communications.
Entre los factores de angiogénesis que estimulan el crecimiento de nuevos vasos se encuentra el factor de crecimiento endotelial vascular (VEGF), que se une a un receptor en las superficies celulares. Esta unión desencadena una secuencia de reacciones químicas dentro de las células que recubren el interior de los vasos sanguíneos, que culmina en el crecimiento de nuevos vasos. Se ha intentado previamente prevenir esta unión atacando al VEGF con anticuerpos o medicamentos, o bloqueando el receptor para que el VEGF no pueda unirse a él. Sin embargo, los tumores responden produciendo más VEGF, lo que abruma tales esfuerzos.
Después de que se produce la unión, una enzima convierte el compuesto fosfatidilinositol-(4,5)-bisfosfato (PIP2) en inositol trifosfato, que es necesario para las reacciones que estimulan el crecimiento de nuevos vasos sanguíneos y el diacilglicerol (DAG). A través de una serie de pasos asistidos por enzimas, el DAG se convierte de nuevo en PIP2, lo que permite su reutilización, según sea necesario.
Los investigadores demostraron que podían detener la angiogénesis bloqueando cualquiera de las enzimas en esta serie de reutilización de PIP2. Primero detuvieron la angiogénesis en cultivos de células humanas y embriones de pez cebra al deshabilitar los genes para una o más de las enzimas. Luego apuntaron a tumores en ratones con medicamentos que bloquean las enzimas de reutilización. En comparación con los ratones normales, los ratones tratados tuvieron menos crecimiento de tumores y vasos sanguíneos tumorales. Además, agregar más VEGF agotó cualquier PIP2 restante, lo que redujo aún más el crecimiento de los vasos sanguíneos.
El Instituto Nacional del Corazón, los Pulmones y la Sangre de los NIH también proporcionó fondos.
QUIÉN:
Brant M. Weinstein, Ph.D., jefe de la División sobre Organogénesis de Vertebrados del NICHD, está disponible para hacer comentarios.
ARTÍCULO:
Stratman AN. Anti-angiogenic effects of VEGF stimulation on endothelium deficient in phosphoinositide recycling. Nature Communications. 2020.
###
Acerca del Instituto Nacional de Salud Infantil y Desarrollo Humano Eunice Kennedy Shriver (NICHD): El NICHD lidera la investigación y la capacitación para comprender el desarrollo humano, mejorar la salud reproductiva, mejorar la vida de niños y adolescentes, y optimizar las habilidades para todos. Si desea más información, visite https://espanol.nichd.nih.gov.
Acerca de los Institutos Nacionales de la Salud (NIH): NIH, la agencia de investigación médica de los EE. UU., incluye 27 institutos y centros, y es un componente del Departamento de Salud y Servicios Humanos de los EE. UU. NIH es la principal agencia federal que realiza y apoya investigaciones médicas básicas, clínicas y traslacionales, y que investiga las causas, los tratamientos y las curas para enfermedades comunes y raras. Para obtener más información sobre los NIH y sus programas, visite https://salud.nih.gov.

 ARRIBA
ARRIBA