Los hallazgos en los cultivos celulares sugieren una posible estrategia para desarrollar tratamientos contra el COVID-19
Crédito: NIAID
Como todos los virus, el SARS-CoV-2 —el virus que causa el COVID-19— depende de las células que infecta para reproducirse. La célula huésped proporciona los componentes y la maquinaria para construir nuevas partículas virales infecciosas. Un nuevo estudio brinda más información sobre la importancia de ciertas modificaciones hechas por la célula huésped a la proteína de espiga del SARS-CoV-2, que el virus usa para ingresar a las células humanas. Estas modificaciones, conocidas como S-acilación, parecen ser críticas para la capacidad del virus de infectar las células. Los hallazgos sugieren que el bloqueo de la S-acilación podría servir como una posible estrategia para desarrollar tratamientos contra el COVID-19.
El estudio fue dirigido por Anirban Banerjee, Ph.D., y Robbins Puthenveetil, Ph.D., de la rama de Biología Estructural y Química de las Proteínas de Membrana del Instituto Nacional de Salud Infantil y Desarrollo Humano (NICHD) Eunice Kennedy Shriver de los NIH. Los investigadores del NICHD y sus colegas del Instituto Nacional del Cáncer de los NIH informaron los hallazgos ![]() en el Journal of Biological Chemistry.
en el Journal of Biological Chemistry.
Antecedentes
Si bien los científicos han aprendido mucho sobre el SARS-CoV-2 desde que surgió el virus en 2019, muchos aspectos de su biología siguen siendo poco conocidos. Una mejor comprensión de los factores que impulsan la replicación y propagación del SARS-CoV-2 puede ayudarlos a identificar nuevos objetivos para posibles tratamientos contra el COVID-19.
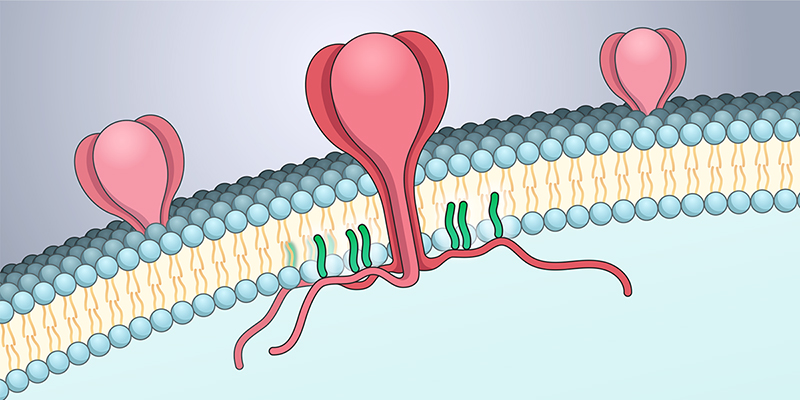
Crédito: Nichole Swan, NICHD
El SARS-CoV-2 usa su proteína de espiga para ingresar a las células humanas y comenzar la replicación viral. La mayor parte de la proteína de espiga sobresale de la superficie del virus, lo que le permite reconocer y unirse a las proteínas en la superficie de las células humanas que infecta el virus. Si bien los científicos han estudiado extensamente la parte externa de la espiga del SARS-CoV-2, se sabe poco sobre la pequeña porción de espiga que reside internamente dentro del virus. En el estudio actual, los investigadores se centraron en esta porción de la proteína.
La S-acilación, en la que los ácidos grasos se unen a las proteínas, puede ser crucial para la función de una proteína. La S-acilación de las proteínas virales se basa en las enzimas (proteínas que facilitan las reacciones químicas) de la célula huésped.
La S-acilación solo puede ocurrir en ciertas zonas de una proteína. La porción interior de la proteína de espiga del SARS-CoV-2 alberga muchos sitios posibles para la S-acilación. El equipo dirigido por el NICHD trató de determinar hasta qué punto se produce la espiga de S-acilación del SARS-CoV-2 y su posible impacto en la capacidad del virus para infectar las células humanas.
Resultados
Los investigadores primero observaron si la espiga de SARS-CoV-2 sufría S-acilación en las células humanas. Los experimentos en cultivos celulares revelaron que sí se produce S-acilación y parece estar concentrada en tres zonas en la parte interior de la espiga. Luego, los investigadores prepararon un conjunto de pseudovirus: virus desactivados que llevan la espiga del SARS-CoV-2 y otras variantes de la espiga diseñadas para carecer de zonas de S-acilación. Descubrieron que la eliminación de las zonas de S-acilación reducía o bloqueaba en gran medida la capacidad de los pseudovirus para infectar las células humanas en cultivo.
A continuación, los científicos buscaron determinar qué enzimas humanas pueden ser responsables de la S-acilación de la espiga del SARS-CoV-2. En las células humanas, la familia zDHHC de 23 enzimas embebidas en la membrana lleva a cabo la S-acilación de proteínas humanas y virales. Una serie de experimentos de cultivo celular reveló 7 enzimas zDHHC que potencialmente están involucradas en la S-acilación de la espiga del SARS-CoV-2.
Finalmente, los investigadores desarrollaron un sistema libre de células que recapitula la S-acilación de la porción interior de la espiga del SARS-CoV-2 por las enzimas zDHHC humanas. Un sistema de este tipo facilitará y agilizará la realización de experimentos para investigar más a fondo los mecanismos detallados de la S-acilación de la espiga del SARS-CoV-2 y para identificar las moléculas que podrían bloquear este proceso.
Importancia
Los resultados brindan más información sobre un aspecto poco conocido de la biología del SARS-CoV-2. También sugieren que el bloqueo de la S-acilación de la proteína de espiga del SARS-CoV-2 podría servir como una posible estrategia de tratamiento contra el COVID-19.
Próximos pasos
Los autores señalan que se necesita más investigación para comprender más a fondo la S-acilación de la espiga del SARS-CoV-2 y su impacto en el virus. El sistema experimental sin células que desarrollaron, junto con imágenes a nivel atómico obtenidas recientemente de dos enzimas zDHHC humanas, ayudará a los investigadores a identificar las moléculas que pueden bloquear la S-acilación de la espiga del SARS-CoV-2 y otras proteínas virales.
Elliot Murphy, Ph.D.; Liam Healy; y Eric Christenson, Ph.D., fueron otros coautores del NICHD que participaron en la redacción del artículo.
Referencia
Puthenveetil, R., et al. S-acylation of SARS-CoV-2 spike protein: mechanistic dissection, in vitro reconstitution and role in viral infectivity ![]() . Journal of Biological Chemistry. DOI: 10.1016/j.jbc.2021.101112
. Journal of Biological Chemistry. DOI: 10.1016/j.jbc.2021.101112 ![]() (2021).
(2021).
###
Acerca del Instituto Nacional de Salud Infantil y Desarrollo Humano Eunice Kennedy Shriver (NICHD): El NICHD lidera la investigación y la capacitación para comprender el desarrollo humano, mejorar la salud reproductiva, mejorar la vida de niños y adolescentes, y optimizar las habilidades para todos. Si desea más información, visite https://espanol.nichd.nih.gov.
Acerca de los Institutos Nacionales de la Salud (NIH): NIH, la agencia de investigación médica de los EE. UU., incluye 27 institutos y centros, y es un componente del Departamento de Salud y Servicios Humanos de los EE. UU. NIH es la principal agencia federal que realiza y apoya investigaciones médicas básicas, clínicas y traslacionales, y que investiga las causas, los tratamientos y las curas para enfermedades comunes y raras. Para obtener más información sobre los NIH y sus programas, visite https://salud.nih.gov.

 ARRIBA
ARRIBA