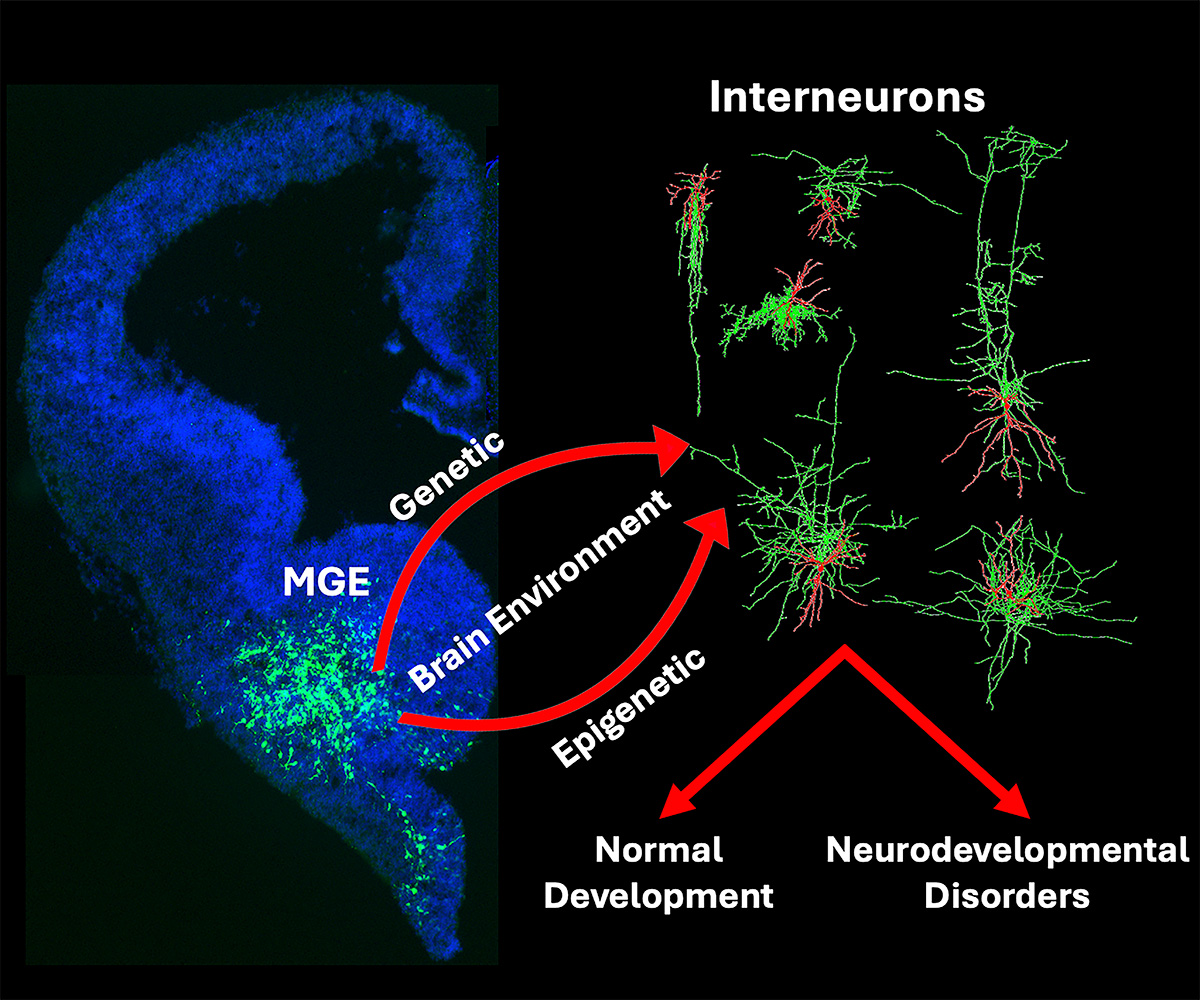
Diagrama que muestra cómo los mecanismos genéticos y epigenéticos influyen en el desarrollo de las interneuronas.
Crédito: Laboratorio Petros
Las interneuronas inhibitorias GABAérgicas son una población celular heterogénea fundamental para establecer el equilibrio excitatorio-inhibitorio adecuado en el cerebro. La disfunción de las interneuronas se asocia a diversos trastornos cerebrales, como la epilepsia, la esquizofrenia y el autismo. Aunque las mutaciones en genes específicos pueden provocar enfermedades, cada vez hay más pruebas de que la alteración de los mecanismos reguladores normales de los genes (es decir, la epigenética) está asociada a muchos trastornos del neurodesarrollo. La metiltransferasa Ezh2 es fundamental para reprimir la expresión génica durante el desarrollo, y a las personas con variantes de EZH2 se les suele diagnosticar el síndrome de Weaver, una enfermedad compleja con discapacidad intelectual. Para explorar la función de Ezh2 en el desarrollo de las interneuronas, el Laboratorio Petros ![]() eliminó Ezh2 específicamente en la eminencia ganglionar medial (EGM), la fuente de muchas interneuronas corticales. La pérdida de Ezh2 en las interneuronas derivadas de la EGM
eliminó Ezh2 específicamente en la eminencia ganglionar medial (EGM), la fuente de muchas interneuronas corticales. La pérdida de Ezh2 en las interneuronas derivadas de la EGM ![]() provocó una variedad de déficits que se destacan a continuación:
provocó una variedad de déficits que se destacan a continuación:
- Los ratones con la mutación de Ezh2 tienen menos interneuronas en el córtex y el hipocampo en comparación con los ratones silvestres. Además, se produjo un cambio en el destino de los subtipos de interneuronas, con una reducción de las interneuronas que expresan parvalbúmina y un aumento de las que expresan somatostatina en los ratones mutantes.
- Aunque las propiedades electrofisiológicas de estas interneuronas eran normales, las interneuronas que expresaban parvalbúmina y carecían de Ezh2 tenían ramas axónicas significativamente más largas y complejas; posiblemente un mecanismo de compensación para la reducción general de este subtipo de interneuronas.
- Los experimentos de secuenciación unicelular en la EGM de ratones silvestres y con la mutación de Ezh2 revelaron cambios tanto en los perfiles de expresión génica como en la accesibilidad de la cromatina que eran predictivos de los cambios observados en el destino celular.
- El análisis de los patrones de metilación de histonas demostró que algunos locus genómicos eran más susceptibles a la pérdida de Ezh2, mientras que otros locus eran más resistentes. Este hallazgo de susceptibilidad diferencial en locus genómicos específicos podría tener consecuencias importantes sobre cómo las perturbaciones epigenéticas se dirigen preferentemente a determinados genes o locus genómicos.
Referencia
Rhodes CT, Asokumar D, Sohn M, Naskar S, Elisha L, Stevenson P, Lee DR, Zhang Y, Rocha PP, Dale RK, Lee S, and Petros TJ. Loss of Ezh2 in the medial ganglionic eminence alters interneuron fate, cell morphology and gene expression profiles ![]() Frontiers in Cellular Neuroscience DOI: 10.3389/fncel.2024.1334244 (2024)
Frontiers in Cellular Neuroscience DOI: 10.3389/fncel.2024.1334244 (2024)
Obtenga más información sobre el Grupo de Afinidad de Neurociencias: https://www.nichd.nih.gov/about/org/dir/affinity-groups/neurosciences ![]()
 ARRIBA
ARRIBA